がん抑制マイクロRNA生合成を制御する分子機構を解明―新たな創薬技術基盤の提示に貢献―
- ヘッドライン
- 記者発表
東京大学
発表のポイント
◆がん抑制機能を持つlet-7マイクロRNAの成熟が、Lin28に依存してTUT4が前駆体let-7(pre-let-7)をウリジル化することで阻害される仕組みを明らかにしました。
◆クライオ電子顕微鏡による構造解析により、Lin28が前駆体let-7の特定の配列を認識し、TUT4をLin28とpre-let7の複合体に引き寄せ、両者が協調してpre-let-7をウリジル化する分子機構を解明しました。
◆本成果は、がん細胞におけるlet-7の発現低下を防ぐ新たな創薬開発につながることが期待されます。

TUT4・Lin28・前駆体let-7 RNAからなる三者複合体構造
発表概要
東京大学大学院新領域創成科学研究科メディカル情報生命専攻の韓 嘯傑(Han Xiaojie)大学院生と富田耕造教授らは、がん抑制機能を持つlet-7 マイクロRNA(miRNA、注1)の発現を抑制する分子機構を解明しました。
let-7は、細胞の過剰な増殖を抑える役割を持つ、代表的ながん抑制miRNAのひとつです。がん細胞では、let-7の前駆体(pre-let-7)は、発現が亢進しているRNA結合タンパク質Lin28に特異的に認識され、Lin28がpre-let-7に結合すると、オリゴウリジル化酵素TUT4がLin28:pre-let-7複合体に引き寄せられ、TUT4:Lin28:pre-let-7三者複合体が形成されます。その結果、TUT4はpre-let-7の3′末端に複数のウリジル(U)を付加し(オリゴウリジル化)、成熟したlet-7 miRNAの生成が阻害されます。Lin28とTUT4によってlet-7の成熟が抑制されると、細胞ががん化しやすくなることが知られています。
本研究では、クライオ電子顕微鏡による構造解析により、Lin28がpre-let-7に結合することで、TUT4が呼び寄せられ、pre-let-7の3′末端がオリゴウリジル化される分子機構を明らかにしました。本成果は、がん細胞における、がん抑制miRNAであるlet-7の発現低下を抑制する作用を持つ新たな創薬開発に貢献することが期待されます。
本研究は、2026年1月12日に『Nucleic Acids Research』誌にオンライン掲載されました。
発表内容
let-7マイクロRNA(miRNA)は、線虫からヒトに至るまで機能的・進化的に保存されているmiRNAであり、幹細胞の分化、発生のタイミング、さらにはがん腫瘍抑制といった重要な生命現象を制御しています。多くのがん細胞ではlet-7の発現低下が確認されており、これが細胞の無制御な増殖の一因となっています。
がん細胞におけるlet-7の生合成は、がん細胞において発現が亢進しているRNA結合タンパク質Lin28に依存して抑制されています。具体的には、Lin28に依存して、ウリジル転移酵素(TUT4)がlet-7の前駆体であるpre-let-7の3′末端に複数のウリジンを付加することで、成熟化let-7の生合成が阻害されます。オリゴウリジル化されたpre-let-7は、その後のDicer(ダイサー、注2)による成熟過程がブロックされ、最終的には分解され、結果として成熟型let-7の発現は著しく低下します(図1)。

図1:がん細胞におけるLin28に依存したlet-7発現抑制機構
がん細胞ではLin28タンパク質が高発現しており、前駆体let-7(pre-let-7)はLin28依存的にウリジル化酵素TUT4によって3′末端に複数のウリジン配列を付加される。その結果、Dicerによる成熟let-7への生合成プロセスが阻害される。ウリジン配列が付加されたpre-let-7は、RNA分解酵素Dis3L2によって分解され、成熟型let-7の発現が著しく低下する。
TUT4はN末端側のLin28と結合するドメイン(Lin28-interacting module: LIM)とC末端側の触媒ドメイン(Catalytic module:CM)からなります(図2a)。また、Lin28はCSD(cold shock domain)と2つのZK(zinc knuckle)ドメインからなります(図2b)。これまで、Lin28とpre-let-7(図2c)の保存されたGGAG配列との相互作用や、TUT4のCMやLIMそれぞれ単独の構造などは明らかにされていましたが、どのようにTUT4がLin28と共同してpre-let-7の3′末端にウリジンを付加するか、その詳細な分子機構は未解明でした。
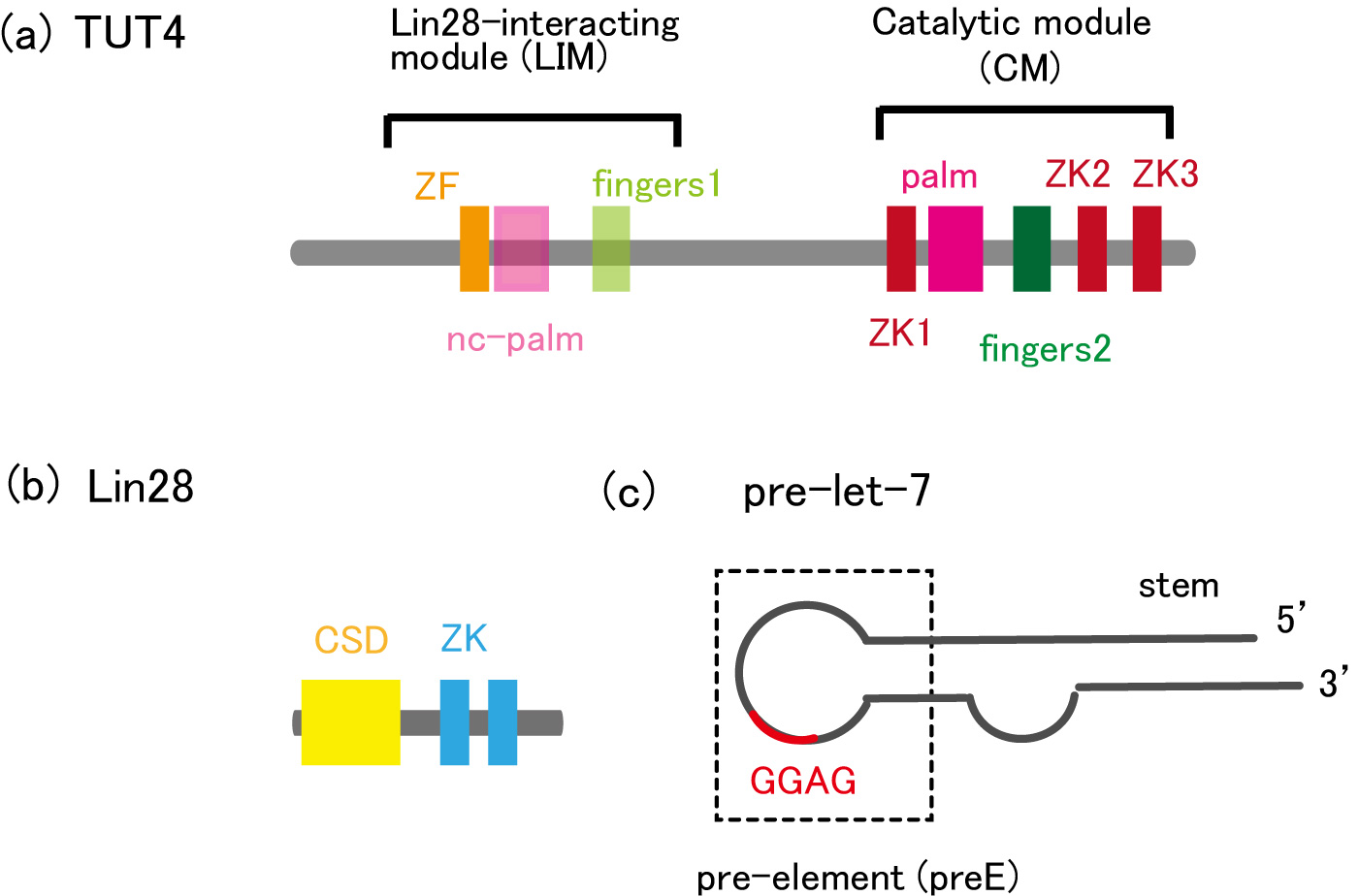
図2:TUT4, Lin28, pre-let7マイクロRNAの構造
(a)TUT4のドメイン構成:Lin28と相互作用するドメインLIM(Lin28 interacting module)、触媒ドメインCM(Catalytic module)。LIMはZF(zinc finger)、nc-palm、fingers1からなり、CMはZK(zinc knuckle)、palm、fingers2から構成される。 (b) Lin28のドメイン構成:CSD(Cold shock domain)、ZK(Zinc knuckle)。(c) 前駆体let-7(pre-let-7):pre-element(preE)内のGGAG配列はlet-7 miRNAで保存されている。
本研究ではヒトTUT4、Lin28、3′末端がオリゴウリジル化されたpre-let7を用いて、Lin28に依存したTUT4によるpre-let-7のオリゴウリジル化の反応状態(伸長段階)を表した、TUT4-Lin28-pre-let-7三者複合体のクライオ電子顕微鏡(cryo-EM)構造解析(注3)、生化学的解析を行いました(図3)。
図3:TUT4:Lin28:pre-let-7複合体の全体構造
その結果、以下の(i)~(iv)が明らかになりました。
i) LIMのZF(Zinc Finger)とLin28のZKは蛋白質間で相互作用すると同時に、pre-let-7のループ内にある保存されたGGAGモチーフを挟み込み、認識している。
ii) LIMとLin28によるRNAを介した相互作用により、pre-let-7がTUT4にリクルートされる。
iii) オリゴウリジル化反応の開始段階と比較すると、今回決定した伸長段階では、CM中のFinger2がpre-let-7の二本鎖部分を掴み、CMとLIMによってpre-let-7:TUT4複合体がより安定化される。
iv) pre-let-7の上部の二本鎖部分は解離し、pre-let-7の3′末端がCMの触媒部位に入り込むことでオリゴウリジル化反応が進行する。
以上より、TUT4のLIMはLin28と協働してpre-let-7の特異的配列を認識し、TUT4に基質であるpre-let-7をリクルートします。また、LIMとCMがpre-let-7の二本鎖部分を認識してTUT4:Lin28:pre-let-7三者複合体を安定化させ、解離しやすいpre-let-7の末端をCM触媒部位に導くことで、Lin28依存的なTUT4によるpre-let-7のオリゴウリジル化反応が進行することが明らかになりました(図4)。
本成果は、がん抑制miRNAの代謝分子機構の理解を深めるとともに、がん細胞におけるmiRNA発現抑制を阻害する新規薬剤や治療法の開発に貢献することが期待されます。

図4:Lin28に依存したTUT4によるpre-let-7のウリジル化分子機構
Lin28とTUT4のLIMが協調してpre-let-7のGGAG配列を認識し、pre-let-7をTUT4にリクルートする。その後、LIMとCMがpre-let-7の二本鎖部分を掴み、ほどけた3′末端がCMの触媒ポケットに導かれて反応が開始される。伸長段階では、二本鎖部分がCMとLIMによってさらに安定に固定され、CMの触媒部位においてウリジル化反応が進行する。
〇関連情報:
Crystal structure of the Lin28-interacting module of human terminal uridylyltransferase that regulates let-7 expression(2019/4/19)
https://www.nature.com/articles/s41467-019-09966-5
発表者・研究者等情報
東京大学大学院新領域創成科学研究科 メディカル情報生命専攻
韓 嘯傑 博士課程
山下 征輔 助教
富田 耕造 教授
論文情報
雑誌名:Nucleic Acids Research
題 名:Mechanistic insights into Lin28-dependent oligo uridylylation of pre-let-7 by TUT4
著者名:Xiaojie Han, Seisuke Yamashita* and Kozo Tomita*
DOI:10.1093/nar/gkaf1421
URL:https://www.doi.org/10.1093/nar/gkaf1421
研究助成
本研究は、日本学術振興会科学研究費助成事業 最先端次世代研究開発プログラム(NEXT program:LS135)、基盤研究A(課題番号:23H00368、18H03980、26251009)、文部科学省科学研究費助成事業 新学術領域研究(課題番号:26113002)国立研究開発法人日本医療研究開発機構(AMED)創薬等ライフサイエンス研究支援基盤事業 創薬等先端技術支援基盤プラットフォーム(BINDS)(課題番号:JP23ama121002)の支援により実施されました。
用語解説
(注1)マイクロRNA (micro RNA:miRNA)
マイクロRNA (microRNA: miRNA)は、長さ約20塩基の非常に短いRNAで、細胞内で遺伝子の発現量を調節する役割を担っています。タンパク質をコードしないものの、標的となるmRNAの分解や翻訳抑制を通じて、細胞の分化・増殖・がん化など、生命活動の根幹に関わるさまざまな生命現象を制御します。
(注2)Dicer(ダイサー)
miRNAは、細胞内で段階的に生合成され、まず数十塩基からなる前駆体miRNA(pre-miRNA)が形成されます。このpre-miRNAを、Dicer(ダイサー)酵素が約20塩基の成熟miRNAに切断・加工することで、遺伝子発現を制御可能な姿へと変換します。
(注3)クライオ電子顕微鏡
試料を極低温で急速凍結し、電子顕微鏡で撮影した多数の画像から3次元構造を高分解能で再構築する技術。タンパク質や複合体の原子レベルの構造解析に用いられる。
関連研究室