「熱」や「痛み」を感じるタンパク質の小さい動きを高速キャッチ! -体に優しい鎮痛薬開発のための新たな創薬指針の提案へ-
- ニュース
- 記者発表
発表のポイント
◆ヒトの熱や痛みを認識するタンパク質TRPチャネルの1分子内部運動を世界で初めて実時間計測し、その運動が極めて小さいことを示しました。
◆TRPチャネルは、唐辛子の成分であるカプサイシンと結合し、右回りねじれ運動を伴って刺激を伝えることを解明しました。
◆TRPチャネルはヒトの痛みのメカニズムに関連しているため、本研究成果は疼痛認識機構の理解や、新しい鎮痛剤の開発等に役立つことが期待されます。
発表概要
東京大学大学院新領域創成科学研究科物質系専攻の佐々木裕次教授、産業技術総合研究所先端オペランド計測技術オープンイノベーションラボラトリバイオ分子動態チーム 三尾和弘ラボチーム長、藤村章子特別研究員、筑波大学計算科学研究センター生命科学研究部門 重田育照教授らの研究グループは、熱や痛みの伝達を司るTRPチャネル(注1)の1分子内部運動を、マイクロ秒オーダーで実時間計測することに世界で初めて成功しました。
ヒト及び多様な動物種の複数の感覚刺激の応答に関与することで知られるTRPチャネルは、4つのサブユニット(注2)から構成され、細胞膜を24回貫通する分子です。最近、詳細な分子構造が決定され、研究が一層加速され注目を集めています。TRPチャネルを活性化させるカプサイシンを添加した実験では、チャネルを開けてイオンを流す動きは、右回りのねじれ運動を伴い、またチャネルを阻害する薬剤を添加した実験では、それと逆向きに左回りのねじれ運動を検出しました。さらにカプサイシンが反応しない変異体TRPチャネルを使った実験では、阻害する薬剤を加えた時と同様にチャネルの運動を抑える左回りのねじれ運動が検出されました。このようにさまざまな条件下でリアルタイムにダイナミックな動きを検出することに成功しました。また、これらの動きがすべて数十pm2/msという極めて小さい拡散定数(注3)で動いていることも判明しました。
本研究グループが用いた計測法は「X線1分子追跡法(Diffracted X-ray Tracking: DXT)」(注4)と呼ばれるもので、金ナノ結晶でラベルされた部位における分子内部動態を1分子動画として検出します。この実験は兵庫県西播磨にある大型放射光施設SPring-8の BL40XU(注5)で行われました。DXTは従来の分子構造決定や反応ポケットの構造解析だけからは得られない、分子の動きに着目した新しい創薬技術の開発への貢献が大いに期待されます。
この成果の詳細は物理化学領域において長い歴史のある国際誌Journal of Physical Chemistryに掲載され、本研究のイメージ図が表紙に採用されました(https://pubs.acs.org/toc/jpcbfk/124/51)。なお、雑誌掲載に先立ち、同誌Webサイトにて、2020年12月9日にオンライン公開されました。
発表内容
本研究で測定されたTRPチャネルは、ヒトに27種類存在し、温度や味覚、細胞内カルシウム濃度など、さまざまな刺激に対するセンサーとして働いています。今回解析に用いたTRPV1は、唐辛子成分であるカプサイシンに反応する辛味受容体であるとともに、熱にも反応して「熱さ」を感じるセンサーでもある興味深い多機能巨大タンパク質分子です。2013年に、クライオ電子顕微鏡(注6)で膜タンパク質として初めて原子分解能構造が報告されるなど、モデルタンパク質としてよく知られています。しかし、細胞膜を20回以上も貫通する複雑な分子構造であるため、チャネル開閉に伴う運動については誰も実時間計測に成功していませんでした。
本研究グループは、静的な分子構造情報に加え、各溶液状態におけるTRP 1分子の内部動態情報が分子機構・解明に極めて重要であると考え、X線1分子追跡法(Diffracted X-ray Tracking: DXT)(図1、図2)を用いて計測・解析を行いました。そしてカプサイシンが反応した際におけるTRPチャネルの分子内部ねじれ運動を可視化することに成功しました。
DXT法は、直径約20ナノメートル(nm)の超微小金ナノ結晶をタンパク質分子の目的部位に化学標識し、運動(方位)をX線・ラウエ斑点(注7)の動きとしてマイクロ秒時分割追跡できる世界で唯一の量子プローブを用いた1分子動態計測です(図2)。本技術は、1998年に東京大学佐々木教授によって考案・実証されました。現在、DXT法は世界最高の精度と最高のフレームレートを誇る1分子動態計測技術で、多くの大型放射光施設から実験室レベルのX線光源を利用した計測まで幅広く利用され始めています。
本研究では、TRPチャネルの細胞外領域を金ナノ結晶で標識し、SPring-8のエネルギーバンド幅の広いX線光源を用いて、1画面を100マイクロ秒の時間分解能でデータ取得を行いました。得られたデータをねじれ運動と傾き運動の2つの回転軸に分解して解析した結果、活性化物質であるカプサイシンを添加した系では、チャネルを開ける動きとして右回りのねじれ運動が、また阻害剤を添加した系では、それと逆向きの運動が生じていることを実時間測定することに成功しました。また、得られたデータが極めて小さい運動であったため、実測時間毎に層別して解析し(ライフタイムフィルタリング法、注8、図3)、結晶構造を用いた理論計算により構造変化の詳細を推定することで、詳細な運動情報を得ることにも成功しました。さらに、カプサイシンとは反応しない変異体タンパク質を使った実験からは、阻害剤を加えた時と同様のチャネルを閉める左回り回転運動が検出されるなど、リアルタイム計測においてTRPチャネルのダイナミックな動きを多面的に示すことができました(図3)。
今回、ライフタイムでデータをグループ化することにより従来観察してきたDXTとは異なる解析方法を採用しました。これまでは運動の大きさを中心にDXT結果の議論が進められていましたが、この手法では初めて、回転方向について極めて詳細に解析ができるようになり、それが先行研究を裏付けられる結果となりました。DXT研究としても、初めて理論計算と比較して実験の正しさを証明することもできました。
TRPチャネルはヒトの痛みのメカニズムに大いに関連しているため、これらの結果は疼痛認識機構の理解や、新しい鎮痛剤の開発等に役立つことが期待されます。また27種あるTRPチャネルの中には、疾病の発症と密接に関係している分子も多いため、DXT計測を通した研究が、それらの治療薬開発に向けて広く貢献すると考えられます。
なお、本研究は、平成30年度(2018年度) 採択の戦略的創造研究推進事業 CREST「計測技術と高度情報処理の融合によるインテリジェント計測・解析手法の開発と応用」(研究総括:雨宮慶幸・高輝度光科学研究センター理事長)における研究課題「クライオ電子顕微鏡法のベイズ高度化と他計測との融合」(研究代表者:光岡 薫・大阪大学教授)及び、国立研究開発法人日本医療研究開発機構(AMED)革新的先端研究開発支援事業(AMED-CREST)「生体恒常性維持・変容・破綻機構のネットワーク的理解に基づく最適医療実現のための技術創出」研究開発領域における研究開発課題「リン恒常性を維持する臓器間ネットワークとその破綻がもたらす病態の解明」(研究開発代表:黒尾 誠・自治医科大学教授)の支援を受けて実施されました。
発表雑誌
雑誌名:「The Journal of Physical Chemistry」(オンライン:12月9日)
論文タイトル:Agonist and antagonist diverted twisting motions of single TRPV1 channel
著者:Shoko Fujimura1, Kazuhiro Mio1*, Masahiro Kuramochi2, Hiroshi Sekiguchi3,
Keigo Ikezaki2, Muneyo Mio1, Kowit Hengphasatporn4, Yasuteru Shigeta4, Tai Kubo1 & Yuji C. Sasaki1,2*
1産総研・東大 先端オペランド計測技術オープンイノベーションラボラトリ、2 東京大学大学院新領域創成科学研究科物質系専攻、3 高輝度光科学研究センター、4筑波大学計算科学研究センター、*:責任著者
DOI番号:10.1021/acs.jpcb.0c08250
アブストラクトURL:http://dx.doi.org/10.1021/acs.jpcb.0c08250
発表者
佐々木裕次(東京大学大学院新領域創成科学研究科物質系専攻 教授)
三尾 和弘(国立研究開発法人産業技術総合研究所 先端オペランド計測技術オープンイノベーションラボラトリバイオ分子動態チーム ラボチーム長)
藤村 章子(国立研究開発法人産業技術総合研究所 先端オペランド計測技術オープンイノベーションラボラトリバイオ分子動態チーム 特別研究員)
重田 育照(筑波大学 計算科学研究センター 生命科学研究部門 教授)
用語解説
注1:TRPチャネル (Transient receptor potential channel)
ショウジョウバエの光応答変異株の原因遺伝子trpのホモログとして、哺乳類で発見された6回膜貫通型陽イオンチャネル。4量体構造を取っていることが確認されています。温度、機械刺激、香辛料、酸-塩基といったさまざまな物理化学的刺激に対するセンサーとして働き、ヒトには27種類のホモログが報告されています。
注2:サブユニット
タンパク質分子は1分子単位で考える場合が多いですが、数個のポリペプチド鎖の組合せと考えることがあります。この各1本のポリペプチド鎖を単位分子のまとまった一部分ずつという意味でサブユニットと呼びます。巨大タンパク質分子の場合は、通常マルチサブユニットから形成されるタンパク質分子です。
注3: 拡散定数
分子内部運動は基本的にブラウン運動で議論します。ブラウン運動とは、液体中の微粒子が不規則に運動する現象で、ロバート・ブラウンによって1827年に発見されました。このブラウン運動の大きさを表現する場合に拡散定数を用いる場合が多くあります。SI単位系における単位は [m2/s]。例えば、0.1ミクロンのエアロゾルの空気中の拡散定数は1ミリ秒あたり0.07μm2です。今回の実験で測定された数値は12.8 pm2/ms 。1ミリ秒あたり12.8 pm2。pmはピコメートルと読み、nm(ナノメートル)の1/1000の単位です。TRPの分子内運動が極めて小さいことが分かります。
注4:X線1分子追跡法 (Diffracted X-ray Tracking; DXT)
数十ナノメートルのナノ結晶をタンパク質に標識し、タンパク質の内部運動に連動したナノ結晶の動きを、X線による回折ラウエ斑点の動きとして高速時分割追跡する手法。佐々木裕次教授が2000年に発表し、今までに多くのタンパク質の内部運動の計測に成功しています(Physical Review Letters, Cell, Sci Rep 等)。
注5:大型放射光施設 SPring-8 (BL40XU)
兵庫県の播磨科学公園都市にある、世界最高性能の放射光を生み出す理化学研究所の施設。(公財)高輝度光科学研究センター(JASRI)が利用者支援等を行っています。SPring-8の名前はSuper Photon ring-8GeVに由来。放射光とは、電子を光とほぼ等しい速度まで加速し、電磁石によって進行方向を曲げた時に発生する、細く強力な電磁波のこと。SPring-8ではこの放射光を用いて、ナノテクノロジー、バイオテクノロジーや産業利用まで幅広い研究を行っています。特に、今回は、同施設のビームライン(BL)の中でも高輝度性を誇るBL40XUを利用しました。
注6:クライオ電子顕微鏡
低温下において、透過型電子顕微鏡(TEM)により多数の均一な粒子を観察、撮影し、画像処理によって粒子の詳細な構造を得る手法。単一の撮影像よりも分解能を向上させることができるほか、さまざまな方向を向いた粒子を撮影することで、3次元立体構造を把握することも可能となりました。低温電子顕微鏡法の利用とともに主にタンパク質などの生体高分子やウイルスなどの解析に用いられ、近年、各種解析手法や検出器の向上により分解能が原子分解能を達成しました。この単粒子解析法開発の功績により、2017年には欧米の研究者3氏にノーベル化学賞が送られました。
注7:X線・ラウエ斑点
X線による回折現象の1つ。X線背面反射法を用いて単結晶体に白色X線を照射した時、ブラッグ角を満足するX線フィルム上の位置に周期的にラウエ斑点が現れます。単色X線を用いる場合は、ブラッグ反射と呼ばれます。
注8: ライフタイムフィルタリング法
これまでのDXT計測の解析おいては、その運動の大きさを比較やスタートするタイミングを議論することで現象を理解してきました。しかし、本研究では運動データを通常よりも極めて多く取得し、それらの回折点移動データを運動速度でふるい分け、その速度分布を議論しました。それがライフタイムフィルタリング法です。その結果、統計的に有意義な議論のできる精度を持って、その分子内部運動が右回りなのか左回りなのかを正確に議論できるようになりました。
添付資料
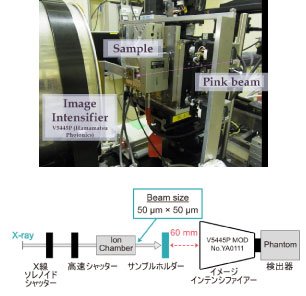
図1:TRPV1のX線実験のセットアップ
エネルギーバンド幅の広いX線を用いて100マイクロ秒/frameの時間分解能でデータ取得を行いました。DXT測定は、Spring-8内の64本のビームラインの中で一番輝度の高いBL40XUを用いました。
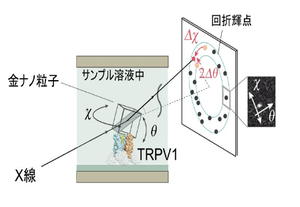
図2:DXTの概要図
TRPV1は水溶液中で活性のある状態で測定しました。TRPV1と金結晶はメチオニンタグ、TRPV1と基盤はヒスチジンタグを用いて特異的に結合させました。X線による金ナノ結晶の回折点を解析しました
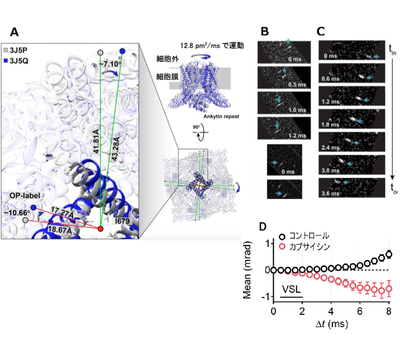
図3:回折点の動く様子と結果
カプサイシンでTRPV1が活性化するときの分子のねじれ運動を、世界で初めて実測に成功。拡散定数で見積もった場合12.8 pm2/msで動いているという結果を得ました(A)。金ナノ結晶から得られる回折点の運動(早く動く回折点(B)と遅く動く回折点(C)の例)をトラッキングし、速度で分類することでTRPV1の回転運動を確認することができました(D)。
記事掲載情報
日経バイオテク https://bio.nikkeibp.co.jp/
医療ニュースQLifePro http://www.qlifepro.com/news/
大学ジャーナルonline https://univ-journal.jp/73751/