合山 進
(ごうやま すすむ/教授/生命科学研究系)
メディカル情報生命専攻/先進分子腫瘍学分野/腫瘍病態学、治療学

略歴
1999年3月東京大学医学部医学科卒業
2006年3月東京大学大学院医学系研究科内科学専攻博士課程修了(医学博士)
2008年2月東京大学医学部附属病院輸血部助教
2009年7月~2015年2月米国シンシナティ小児病院医療センター客員研究員
2015年3月東京大学医科学研究所准教授
2020年4月より現職
教育活動
大学院:CBMS基礎講義III, CBMS発展講義VII
研究活動
近年の様々な技術革新により、「がんを治す」ことは遠い未来の夢ではなく、現実的な目標となりました。私達の研究室では、造血器腫瘍を中心に、がん病態生理の解析と新規治療法の開発を行っています。
(1) がん幹細胞と腫瘍免疫
がんの発症、再発の根源である「がん幹細胞」を駆逐しない限り、がんを治すことはできません。私達は、がん幹細胞が抗がん剤や腫瘍免疫に抵抗性を示すメカニズムを調べています。最近では、白血病幹細胞が腫瘍免疫の攻撃から逃れることでp53活性化薬に治療抵抗性を示すことを明らかにしました(図1)。
(2) クローン性造血の制御を介した疾患予防法の開発
最近、遺伝子変異を持つ異常な血液細胞が増殖する「クローン性造血」が、高齢者では一見健康な人にも高頻度に認められることがわかってきました。私達は、特定の遺伝子変異がクローン性造血を促進するメカニズムを解明し、加齢に伴う様々な疾患の予防に役立てたいと考えています。
(3) タンパク質工学に基づく創薬研究
転写因子やエピゲノム因子は、がんが発症し進展していく過程で中心的な役割を果たしていますが、これらの多くは阻害剤の開発が難しい“undruggable”な分子と考えられています。私達は最新のタンパク質間相互作用制御技術を用いて(図2)、転写・エピゲノム制御因子を標的とする治療薬の開発に挑んでいます。
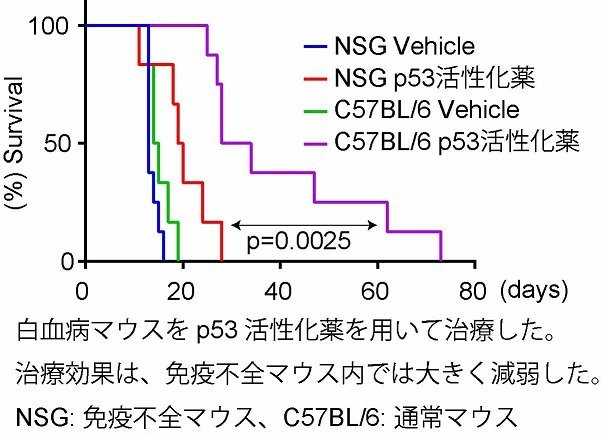
図1.腫瘍免疫は白血病マウスに対するp53活性化薬の治療効果を増強する
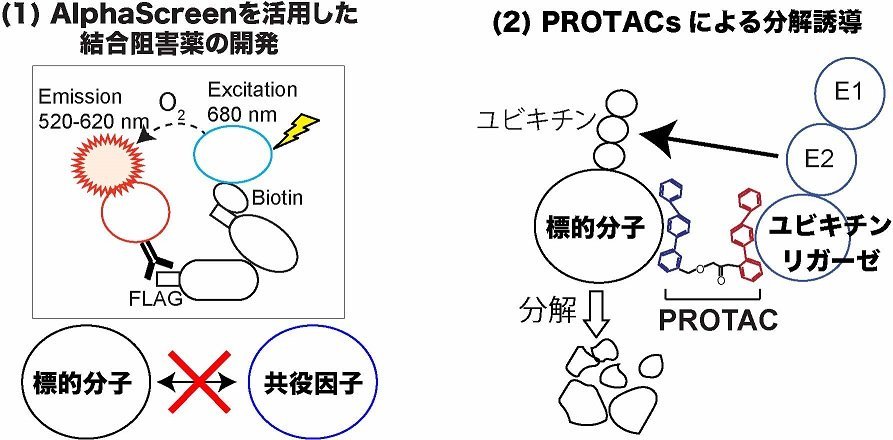
図2.タンパク質間相互作用制御技術を用いた創薬研究
文献
1)Hayashi Y, *Goyama S, Liu X, Tamura M, Asada S, Tanaka Y, Fukuyama T, Wunderlich M, O’Brien E, Mizukawa B, Yamazaki S, Matsumoto A, Yamasaki S, Shibata T, Matsuda K, Sashida G, Takizawa H, *Kitamura T. Antitumor immunity augments the therapeutic effects of p53 activation on acute myeloid leukemia. Nature Communications 10(1): 4869 (2019).
2) Asada S, Goyama S, Inoue D, Shikata S, Takeda R, Fukushima T, Yonezawa T, Fujino T, Hayashi Y, Kawabata KC, Fukuyama T, Tanaka Y, Yokoyama A, Yamazaki S, Kozuka-Hata H, Oyama M, Kojima S, Kawazu M, Mano H, *Kitamura T. Mutant ASXL1 cooperates with BAP1 to promote myeloid leukaemogenesis. Nature Communications 9(1): 2733 (2018).
3) Goyama S, Yamamoto G, Shimabe M, Sato T, Ichikawa M, Ogawa S, Chiba S, *Kurokawa M. Evi-1 is a critical regulator for hematopoietic stem cells and transformed leukemic cells. Cell Stem Cell 3(2): 207-220 (2008).
4) Goyama S, Schibler J, Cunningham L, Zhang Y, Rao Y, Nishimoto N, Nakagawa M, Olsson A, Wunderlich M, Link KA, Mizukawa B, Grimes HL, Kurokawa M, Liu PP, Huang G, *Mulloy JC. Transcription factor RUNX1 promotes survival of acute myeloid leukemia cells. Journal of Clinical Investigation 123(9): 3876-88 (2013).
その他
日本血液学会評議員(2016年~現在)、日本内科学会、日本癌学会、ISEH各会員。
将来計画
これまでに得た腫瘍病態生理に関する知見を基に、新しい治療薬、もしくは治療戦略を開発します。特に、タンパク質間相互作用(Protein-Protein Interaction: PPI)制御技術を活用した創薬に力を入れています。
教員からのメッセージ
結果にコミットします!皆さん一人ひとりが自分で実験をし、それを論文にできるようサポートします。
